医疗器械临床试验
定义:通过人体测试验证器械安全性与有效性,通常分三阶段:
Ⅰ期:初步评估器械的基本安全性与操作性能;
II.期:验证有效性并优化使用参数;
III.期:确证安全有效性,支撑注册上市
多中心试验:可同时开展多中心的器械临床试验
方案设计:根据医疗器械产品特点、预期用途和目标人群,设计科学合理的临床试验方案。
数据管理:采用先进的数据管理系统,确保数据的完整性、准确性和安全性。
统计分析:统计分析团队经验丰富,提供科学、严谨的统计分析报告。
项目管理:制定详细的项目计划,明确各个阶段的任务和时间节点,并定期进行项目进度评估和风险预警。
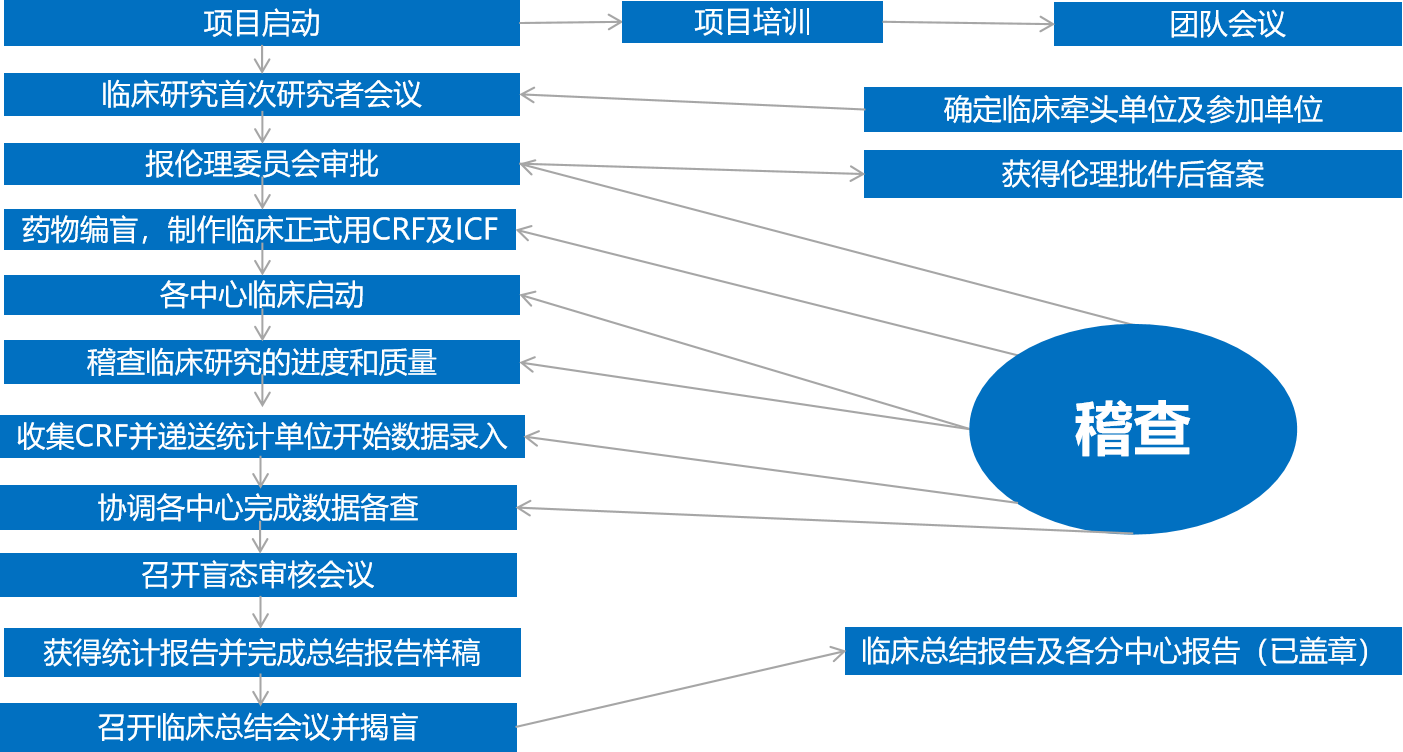
质量控制:严格按照GCP标准和内部SOP对试验过程进行稽查,确保每个环节都符合法规要求。
专业团队:高素质专业团队包括临床医学专家、数据管理人员、统计分析师以及项目管理人员,且均具有丰富的医疗器械临床试验经验。
丰富的项目经验:完成医疗器械临床试验30+例,涵盖多种医疗器械产品,包括诊断设备、治疗器械、植入性器械等,适应症包括心血管、外科、术中止血、检测试剂盒、医美等多方面。
健全的质量控制体系:稽查部门独立于项目部,在不同阶段定期对临床试验进行稽查,及时发现并解决潜在问题,确保真实性和可靠性。
高效的项目管理能力:详细的项目计划,明确各阶段的任务和时间节点,定期项目进度评估和风险预警。与客户保持密切沟通,及时向上反馈项目进展情况。
广泛的临床试验网络:在全国多省市拥有多个优质合作的临床试验机构,这些机构均符合GCP标准,能够为您的医疗器械临床试验提供坚实的基础保障。我们能够协调多个中心的资源,确保试验的同步推进。