上市后临床试验
I-III期注册临床试验
政府事务
其他相关业务
业务介绍:
- 公司可承接上市后全链条临床服务,覆盖中药品种保护临床试验;上市后临床推广—临床指南/专家共识;国家及省部级科研课题临床试验;学术论文发表、医疗机构准入等临床;
- 以合规体系、专业能力与全国资源为依托,为客户提供高效、稳定、可落地的上市后临床与学术增值服务;
核心优势:
- 专业团队:医学、临床、数据、统计组成全链条团队;
- 高效执行:项目管理工具实时监控进度与风险;项目文件夹云盘共享,授权项目成员可通过电脑或手机实现数据、文件、图片等资料的实时浏览、上传及下载;
- 临床试验网络:在全国多省市拥有多个优质合作的临床试验机构,符合GCP标准,确保试验合规且快速推进;
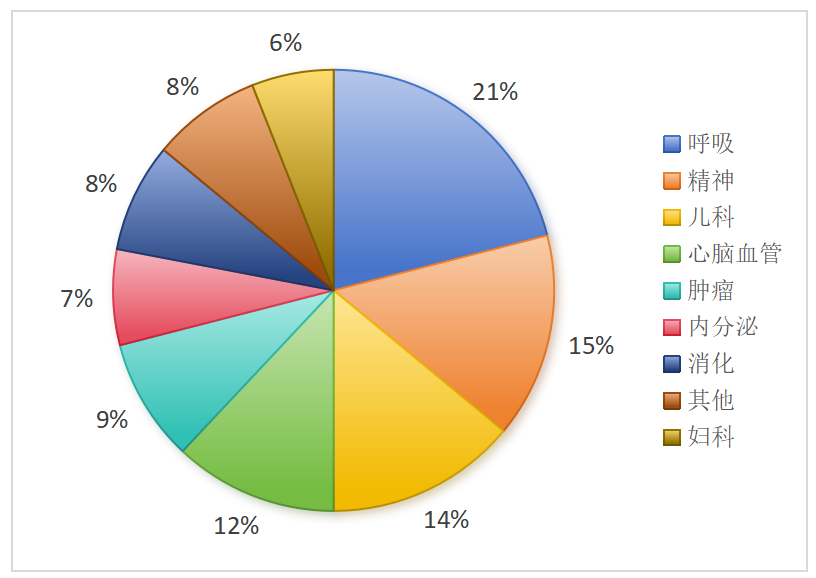
- 经验丰富:覆盖呼吸、心脑血管、内分泌、妇科、儿科、泌尿、消化、骨科、耳鼻咽喉、皮肤、血液、肝病等诸多领域;
部门简介:
公司设立药政事务部,全面统筹中药全生命周期注册管理与政策事务,以专业法规能力与丰富实操经验为支撑,深度衔接药品研发与监管政策,为产品布局、品种培育及产业高质量发展提供坚实、高效、全链条的合规保障。
业务涵盖:
- 中药创新药注册申报:涵盖中药1类创新药、中药2类改良型新药研发注册,以及医疗机构中药制剂向创新药转化的全流程申报服务;
- 中药上市后:包括处方药转非处方药(OTC)申报、药品补充申请、说明书修订、适应症及适用人群范围优化等合规变更工作;
- 中医药领域科研课题申报:聚焦国家及地方中医药管理局等主管部门课题,提供方案策划、材料编制与申报落地支撑;
- 医疗机构中药制剂研发与备案申报:提供从处方梳理、工艺研究到申报落地的全链条服务,助力院内制剂规范化发展;
- 中药品种保护申报及后续维护,助力核心品种获得政策保护与市场优势;